Wie beschichtet man ein Metall mit einem anderen? Durch Galvanisieren!
Nicht alles, was glänzt ist Gold! Oder Kupfer, oder… Die Oberflächen vieler Gegenstände sind nur mit einer dünnen Schicht dieser wertvollen Metalle überzogen. Solche Dinge nennt man dann vergoldet, verkupfert, versilbert oder ähnlich. Doch das bedeutet nicht, dass solche Gegenstände minderwertig sind. Vielmehr wird ihre Haltbarkeit durch ihre besonder Metalloberfläche verbessert – und sieht auch noch hübsch aus. Denn eine Edelmetall-Schicht ist reaktionsträge und schützt den Gegenstand unter ihr vor den Kräften von Wind und Wetter. Aber wie bringt man eine dünne Metallschicht auf ein anderes Material?
Dazu wird Wanderlust geladener Metallteilchen (sogenannter Metall-Ionen) ausgenutzt – und das könnt ihr leicht selber machen!
Ihr braucht dazu
- Eine Sicherheitsnadel
- Eine Kupfermünze (z.B. 1,2 oder 5 Eurocent)
- Eine Kleine Schale
- Haushaltsessig
- Soda oder Natron (für die Entsorgung)
Sehr dreckige Münzen könnt ihr mit Essig und etwas Kochsalz leicht reinigen – wie genau das geht, zeige ich euch hier.

So geht’s
Lest in jedem Fall den Abschnitt „Entsorgung“ durch, bevor ihr mit dem Experimentieren beginnt! Nach dem Versuch ist nämlich ein besonderer Entsorgungsschritt nötig. Den könnt ihr euch wesentlich leichter machen, wenn ihr von vorneherein sparsam arbeitet.
- Legt Münze und Nadel nebeneinander in die Schale, sodass sie sich nicht berühren!
- Gebt so viel Essig dazu, dass beide Teile vollständig bedeckt sind. Verwendet dabei so wenig Essig wie möglich – denn je weniger Essig ihr später entsorgen müsst, desto weniger Soda oder Natron werdet ihr dafür brauchen!

- Wartet ein paar Tage und schaut ab und zu nach, was sich verändert.
- Wenn euch der Essiggeruch stört, könnt ihr die Schale einfach abdecken (mit einem Brett, einem Buch oder Ähnlichem)
Das könnt ihr beobachten
Die Nadel färbt sich mit der Zeit kupferrot, während die Münze zunehmend matt wird. Der Essig färbt sich zudem gelbgrün.
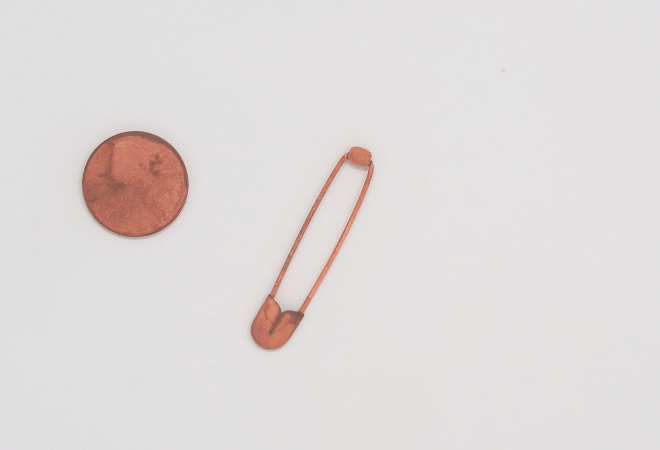
Das passiert
Haushaltsessig besteht aus Wasser und Essigsäure. Kommt ein Metall wie Kupfer mit einer Säure in Berührung, geben stets ein paar Metallatome an der Oberfläche ein oder mehrere Elektron(en) ab. Dabei verlassen die Atome – welche zu Ionen werden – die Metalloberfläche und lösen sich im Wasser.
Das „(aq)“ in der Gleichung bedeutet „in Wasser gelöst“.
Da Kupfer ein ziemlich edles Metall ist, können zunächst nur sehr wenige seiner Atome auf diese Weise zu Ionen werden. Diese wenigen Ionen können sich jedoch frei im Wasser bewegen – und so irgendwann an die Oberfläche der Sicherheitsnadel, die aus Stahl bestehen mag, gelangen.
Stahl wiederum enthält Eisenatome. Und Eisenatome geben sehr viel leichter Elektronen ab als Kupferatome.
So kommt es, dass die Eisenatome ihre Elektronen liebend gern an Kupferionen abgeben.
Die Eisenatome werden dabei zu Ionen, die sich im Wasser lösen, während die Kupferionen wieder zu Kupfer-Atomen werden, die sich an der Eisenoberfläche niederlassen.
Sobald auf diese Weise Kupfer-Ionen aus der Lösung verschwinden, bleibt darin „Platz“ für neue Kupfer-Ionen. Die können sich somit von der Münze lösen und ihre Wanderung in Richtung Sicherheitsnadel antreten. (Alle beteiligten Reaktionen sind sogenannte Gleichgewichtsreaktionen. Le Châtelier erklärt hier am Flughafen, was es damit auf sich hat und wie die Richtung, in der sie ablaufen, von den Mengen der beteiligten Teilchen abhängt!)
Geladene Teilchen, die wandern, sind „Strom“
Geladene Teilchen, die wandern? Ja, ihr denkt richtig: Das ist nichts anderes als elektrischer Strom! Der Versuchsaufbau ist eine Art simple Batterie. Die Ionen wanderen darin so lange von der Münze zur Nadel, bis die ganze Nadeloberfläche mit Kupferatomen bedeckt ist. Dann gibt es dort nämlich keine Eisenatome mehr, die ihre Elektronen an weitere Kupferionen abgeben könnten. Die Batterie ist „leer“.
Galvanisieren im „richtigen Leben“
Wer Gegenstände mit einer edlen Metallschicht verkaufen möchte, mag in der Regel nicht tagelang warten, bis das Galvanisieren weit genug vorangeschritten ist. Deshalb benutzt er zum Einen statt Essig eine Lösung, die bereits reichlich Kupfer-Ionen (oder andere gewünschte Metall-Ionen) enthält. Zum Anderen schliesst er seine Anlage an elektrischen Strom an: Das Kupfermetall an den (physikalischen) Pluspol, das Material, das verkupfert werden soll, an den Minuspol.
Die angeschlossene Stromquelle liefert zusätzliche Elektronen in das zu verkupfernde Material, die die Kupferionen entgegen nehmen können. Zudem ermöglicht die Stromquelle den vom Kupfer abgegebenen Elektronen das Abfliessen, sodass auch leicht neue Kupfer-Ionen in Lösung gehen können.
Und zu guter Letzt leitet Kupfer selbst den Strom sehr gut. Das heisst, die zusätzlichen Elektronen gelangen auch leicht durch die neu entstehende Kupferschicht, sodass diese so lange dicker wird, wie die Stromquelle angeschlossen ist.
Vom Galvanisieren zur nutzbaren Batterie
Wenn ihr euch die oben beschriebenen Reaktionen genau anschaut, werdet ihr feststellen, dass dabei in der Kupfermünze Elektronen „übrig“ bleiben, in der Eisennadel aber nicht. Im Kupfer sammeln sich demnach mehr Elektronen als im Eisen. Verbindet man aber mit einem leitfähigen Material eine Elektronenansammlung mit einem Ort mit wenig Elektronen, so fliessen Elektronen von der Ansammlung zum „leeren“ Ort ab. Und fliessende geladene Teilchen kennen wir als elektrischen Strom!
Unser Aufbau mit Münze und Sicherheitsnadel, die lose in Essig liegen, ist als Batterie aber ziemlich unpraktisch. Denn auch der Essig ist elektrisch leitfähig und bildet, sobald Münze und Nadel vollständig eingetaucht sind, eine unumgängliche Abkürzung für den Strom.
Die könnt ihr vermeiden, indem ihr eure Metalle nicht in einer Flüssigkeit, sondern in einem festen Material, in dem auch Ionen wandern können, unterbringt. Zum Beispiel in einer Kartoffel. Wie ihr aus Kartoffeln wirklich funktionierende Batterien bauen könnt, zeige ich euch hier!
Entsorgung
Der Essig enthält nach dem Galvanisieren Kupferionen (sie geben der Flüssigkeit die grünliche Farbe), die giftig für Wasserorganismen sind und deshalb nicht ins Abwasser dürfen. Verwendet deshalb so wenig Essig wie möglich. Gebt nach dem Versuch, wenn ihr Nadel und Münze aus der Schale genommen habt, feste Soda oder Natron zu dem Essig darin. (Achtung! Geht langsam vor und rührt zwischendurch um! Die Mischung schäumt kräftig und wird warm: Allein das ist schon ein chemisches Spektakel, das schnell zur Sauerei ausarten kann!)
Mischt so lange Soda oder Natron mit dem Essigrest, bis keine Reaktion mehr sichtbar ist. Dann habt ihr die Säure neutralisiert. Mit noch ein wenig mehr Soda oder Natron wird die Lösung basisch: Das ist euer Ziel. Die Kupferionen bilden nämlich bei basischem pH-Wert ein Gemisch fester Stoffe (in eurer Schale vor allem Kupferacetat, Kupfercarbonat und Kupferhydroxid), das man Grünspan nennt.
Gebt das Gemisch aus festen Stoffen und Flüssigkeit durch ein Filterpapier (z.B. einen Kaffeefilter) und lasst das Papier mitsamt den Feststoffen trocknen, bevor ihr es in den Hausmüll gebt. Die filtrierte Lösung darf dann mit viel Wasser in den Ausguss.
Nun wünsche ich euch viel Spass beim Galvanisieren!










