Magnete – wer kennt sie nicht. Harte, dunkle Gegenstände, scheinbar weder ganz Stein noch ganz Metall, von welchen geheimnisvolle Kräfte ausgehen. Schon in meiner frühen Kindheit waren sie nicht aus dem Spielzimmer weg zu denken – hielten sie doch die Waggons meiner Holzeisenbahn zusammen, und ermöglichten einem Kleinkind dennoch, den Zug nach Belieben wieder auseinander zu nehmen.
Noch spannender fand ich dereinst jedoch, die Waggons mit den „falschen“ Enden zueinander auf die Gleise zu stellen und einen auf den anderen zuzuschieben, sodass der zweite Waggon wie von Geisterhand vor dem ersten zurückwich…
In der Welt der Grossen sind hingegen Kühlschrankmagnete nicht wegzudenken, oder ebensolche im Büro oder der Schule am Whiteboard. Oder als praktische Scheibenwischer in einer gläsernen Hermetosphäre. Oder…Verwendung für Magnete gibt es in zahllosen Varianten. Und wer zwei davon aufeinander zu bewegt, kann die geheimnisvolle Abstossung spüren, die ich schon als Kind an der Holzeisenbahn beobachten konnte.
Seit meiner Kinderzeit hat sich überdies die Erscheinung mancher Magnete geändert. Sie scheinen kleiner geworden zu sein – und ihre Kräfte gleichzeitig stärker, und häufig schimmern sie metallisch silbern. „Supermagnete“ werden diese Kraftpakete oft genannt, und aus seltenen Erden sollen sie bestehen.
Doch wie und wo entstehen die mysteriösen Kräfte der Magnete eigentlich? Was ist „Magnetismus“? Was hat Magnetismus mit Strom zu tun? Welche Stoffe sind magnetisch? Warum sind Supermagnete so stark? Und wie kann ein Supraleiter über einem Magneten schweben?
Was hinter den Kräften steckt
Hast du zwei Magnete zur Hand? Oder einen Magnet und ein Stück Eisen? Wenn du beide langsam aufeinander zu bewegst, wirst du schnell feststellen, dass die geheimnisvollen Magnet-Kräfte umso stärker werden, je näher das eine dem anderen kommt. Irgendetwas ist also im Raum um den Magnet herum, das ein Stück Eisen zu ihm hin zieht – und zwar immer schneller, je näher es dem Magnet kommt. Die Physiker nennen dieses Etwas Magnetfeld.
Was ist ein Magnetfeld?
Ein „Feld“ nennen die Physiker die räumliche Verteilung einer physikalischen Grösse. Das heisst, diese Grösse hat an jedem Punkt in einem Raum einen bestimmten Wert – das Feld ist die Gesamtheit dieser Werte. Würde man draussen, wenn es kalt ist, ein Lagerfeuer entzünden und an jedem Punkt in der Umgebung die Temperatur messen, könnte man die gesammelten Werte zu einem Temperaturfeld zusammenfassen und seine „Gestalt“ beschreiben: Je näher ein Punkt im Temperaturfeld am Feuer liegt, desto höher wird die Temperatur sein.
Neben solch einfachen Grössen wie der Temperatur (Mathematiker nennen solche Grössen „skalar“) gibt es andere physikalische Grössen, die neben ihrem Wert auch eine Richtung haben (solch eine Grösse nennen die Mathematiker „Vektor“): Die Schwerkraft bewegt Gegenstände überall auf und über der Erde nach „unten“, das heisst in Richtung Erdmittelpunkt, ein Zug fährt mit einer bestimmten Geschwindigkeit geradeaus (während die Geschwindigkeit des gleichschnellen Gegenzugs wohl den gleichen Wert hat, aber die entgegengesetzte Richtung).
Auch die geheimnisvolle Kraft im Magnetfeld hat an jedem Punkt eine Richtung. Um die Verteilung der Richtungen im Raum darzustellen zeichnet man Linien, die den Verlauf der Richtungen andeuten: Ein magnetischer Gegenstand ( auf welchen die „Magnetkraft“ wirkt), wird im Magnetfeld entlang dieser „Feldlinien“ bewegt.
Ein Magnetfeld ist also die Gesamtheit aller Werte und Richtungen für die „Magnetkraft“ in der Umgebung eines Magneten. Zumindest für die Mathematiker. Für die Physiker ist ein Magnetfeld jedoch mehr als eine Sammlung von Zahlen: Es ist wirklich da – ein existierendes physikalisches Etwas, dem Energie innewohnt und das sich mit Hilfe von Gleichungen beschreiben lässt (Felder im Allgemeinen sind tatsächlich „nur“ Zahlensammlungen – reale Felder wie das Magnetfeld sind unter diesen etwas Besonderes).
Die Gleichungen für Magnetfelder hat der Physiker James Clerk Maxwell aufgestellt – deshalb werden sie nach ihm „Maxwell-Gleichungen“ genannt. In Worten sagen sie in etwa Folgendes über Magnetfelder aus:
- Ein Magnetfeld hat weder Ursprung noch Ende – es ist quellenfrei. Die „Pole“ eines Magneten markieren also nur die Orientierung des Magnetfelds – welches sich folglich auch im Magneten selbst erstreckt. Dementsprechend sind auch die Magnetfeldlinien ohne Anfang und Ende – sie sind in sich geschlossen, wie eine Rundstrecke beim Autorennen.
- Verändert sich ein Magnetfeld mit der Zeit, entsteht dadurch ein elektrisches Feld mit in sich geschlossenen Linien. Magnetismus ist also stets eng verbunden mit der Elektrizität – und umgekehrt.
- Denn eine weitere Gleichung sagt aus, dass elektrische Ströme bzw. die Veränderung eines elektrischen Feldes stets ein Magnetfeld erzeugen.
- So wird die Maxwell-Sammlung denn auch durch eine vierte Gleichung zu elektrischen Feldern (welche damit auch „real“ sind) vervollständigt: Ein elektrisches Feld kann einen Ursprung haben: Es geht von einer elektrischen Ladung aus. Die Feldlinien verlaufen dann von dieser Ladung fort. Das heisst, es gibt elektrische Felder mit nur einem Pol (der entweder positiv oder negativ ist), während Magnetfelder zwecks Darstellung ihrer Orientierung stets zwei Pole haben!
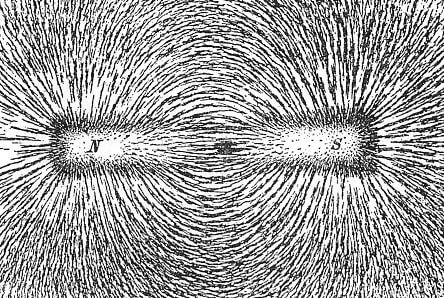
Eisenfeilspäne richten sich entlang von Magnetfeldlinien zwischen Nord- und Südpol eines Magneten aus und machen das Feld auf diese Weise „sichtbar“.(von Berndt Meyer [GFDL oder CC BY-SA 3.0], via Wikimedia Commons)
Als Pole eines Gegenstands, welcher ein Magnetfeld erzeugt, werden somit die Bereiche bezeichnet, in welchen die Magnetfeldlinien aus dem Gegenstand aus- bzw. wieder in ihn eintreten. Dabei hat man sich darauf geeinigt, dass die Seite, an welcher die Feldlinien austreten, sich im Magnetfeld der Erde nach Norden ausrichtet – und dementsprechend Nordpol heisst (der Nordpol der Erde ist also ein magnetischer Südpol, denn entgegengesetzte Pole ziehen sich an). Dort, wo die Feldlinien in den Magneten eintreten, ist dementsprechend der Südpol des Magneten.
Ein Magnetfeld ist also die räumliche Verteilung einer Kraft, die auf magnetische und magnetisierbare Materie und elektrische Ladungen wirkt: An jedem Punkt im Magnetfeld hat die Kraft einen bestimmten Wert (eine „Feldstärke“) und eine bestimmte Richtung.
Woher kommt die Magnetkraft?
Mit unseren Augen in unserer Welt betrachtet erscheinen die Magnetkräfte mystisch – ganz wie die elektrischen Kräfte, die beispielsweise einen Luftballon an der Wand festhalten, nachdem man ihn am Wollpullover gerieben hat. Und ganz wie die elektrische (Elementar-)Ladung ist auch der Magnetismus eine Eigenschaft der kleinsten Teilchen:
Jedes Proton, Neutron und Elektron ist ein winzig kleiner, unvorstellbar schwacher Magnet (diese Eigenschaft eines Teilchen wird auch magnetisches Moment oder kurz „Spin“ genannt)! Und diese winzigen Magnete lassen sich zu grösseren Magneten zusammensetzen, wobei ihre Magnetkräfte sich addieren: Die Protonen und Neutronen, die einen Atomkern bilden, machen den Kern zu einem etwas grösseren Magneten. Die Elektronen der Atomhülle jedoch steuern den Löwenanteil zum Magneten vom Ausmass eines ganzen Atoms bei. Atome verbinden sich zu Molekülen oder Kristallen – und Atom-Magnete vereinen sich Stoffen, die wir sehen und anfassen und deren Magnetkräfte wir wahrnehmen können.
Warum sind dann nicht alle Stoffe magnetisch?
Jeder der kleinen Elementarteilchen-Magnete (oder kurz: Elementarmagnete) erzeugt sein eigenes winziges Magnetfeld. Und das hat, wie oben beschrieben, eine bestimmte Orientierung. Das heisst, der Nordpol des kleinen Magnetfelds weist in eine bestimmte Richtung, der Südpol in die Gegenrichtung. Und wenn man Richtungen addiert, kommt nicht immer das raus, was man von der Addition von blossen Zahlen gewohnt ist.
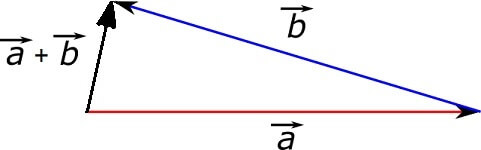
Addition von Vektoren: Die Länge der Pfeile stellt den Wert der Grössen a und b dar, die Pfeilrichtung die zur Grösse gehörende Richtung. Solche Vektoren werden addiert, indem man die Pfeile Schaft an Spitze aneinanderreiht. Unterscheiden sich die Richtungen der Summanden dabei sehr, ist der Wert der Summe (die Länge des schwarzen Pfeils) mitunter kleiner als die Werte der Summanden.
Wenn man Grössen mit gar zu unterschiedlichen Richtungen addiert, ist das Ergebnis mitunter kleiner als die Summanden! Und wenn man nur genug Summanden mit unterschiedlichen Richtungen addiert, ist das Ergebnis schliesslich praktisch null.
Die Elementarmagnete in einem Stoff können ihre Orientierung frei wählen – so wie eine Kompassnadel sich frei um ihre Mittelachse drehen kann. So orientiert sich jeder Elementarmagnet in einem Stoff wie er gerade will – und wenn genug Elementarmagnete zusammenkommen, wird die Summe ihrer Orientierungen praktisch null: Es entsteht kein wahrnehmbares, „grosses“ Magnetfeld.
Erst wenn Elementarmagnete in ein bereits bestehendes Magnetfeld geraten, zeigen sich Unterschiede zwischen den magnetischen Eigenschaften der Stoffe. Magnetismus ist also nicht gleich Magnetismus. Stattdessen gibt es:
Diamagnetismus
Sobald Elementarmagnete in ein „fremdes“ Magnetfeld geraten, richten sie sich entlang der Feldlinien aus, wie Kompassnadeln im Erdmagnetfeld. Und sobald Ordnung herrscht, wird die Summe der kleinen Magnetfelder zu einem spürbar Grossen – allerdings dem „fremden“ Magnetfeld entgegen gerichtet. Die Magnetkraft, die der Stoff erst im „fremden“ Magnetfeld erhalten hat, hebt die Wirkung ebendieses fremden Magnetfeldes folglich (teilweise) auf.
Da Magnetfeldlinien jedoch nicht einfach unterbrochen werden dürfen, lässt sich dies darstellen, indem man die Feldlinien um den Stoff im Magnetfeld herum führt, als würde der Stoff die Linien verdrängen. Tatsächlich werden solche diamagnetischen Stoffe aus einem Magnetfeld hinausgedrängt wie ein Schwimmer aus dem Wasser!

Kohlenstoff ist diamagnetisch: Ein Graphit-Plättchen schwebt im gemeinsamen Magnetfeld von vier vergoldeten Neodym-Magneten
Da die Elektronen unter den Elementarteilchen den Löwenanteil an den magnetischen Eigenschaften eines Stoffes haben, sind für dieses Verhalten im Magnetfeld nur Elektronen nötig – und die gibt es in jedem Atom. Daher ist jeder Stoff, der aus Atomen besteht, ein Diamagnet. Bemerkbar macht sich der Diamagnetismus allerdings nur, wenn der Stoff keine weitere, stärkere magnetische Eigenschaft hat- zum Beispiel bei Wasser oder bei Kohlenstoff.
Die Tatsache, dass damit zwei der wichtigsten Bestandteile von Mensch und Tier diamagnetisch sind, hat die Fantasie einiger Wissenschaftler angeregt: Was wäre, wenn wir dank unseres Diamagnetismus‘ auf Magnetfeldern durch die Luft schweben könnten? Einem Frosch ist ebendies dank eines richtig starken Magnetfelds bereits gelungen (wenn auch mit Sicherheit nicht freiwillig):
Dem Frosch ist dabei übrigens nichts passiert. Magnetfelder sind sowohl für Frösche als auch für Menschen nicht direkt spürbar. Ein ausreichend starker Magnet, dessen Feld einen ganzen Menschen in die Luft drängen kann, muss jedoch erst noch gebaut werden.
Paramagnetismus
Während alle Atome Elektronen haben, haben nicht alle Atome automatisch ein magnetisches Moment. Denn zu einem solchen kommen sie nur, wenn sich die Orientierungen der magnetischen Momente ihrer Bestandteile – insbesondere der Elektronen – nicht gegenseitig aufheben.
Wenn Atomen ein eigenes magnetisches Moment gegeben ist, richten sie sich in einem „fremden“ Magnetfeld geordnet aus wie alle anderen Elementarmagnete auch – allerdings verläuft das Magnetfeld, das sie so gemeinsam bilden, parallel, also ebenso orientiert wie das „fremde“ Magnetfeld. Die Folge davon: Innerhalb eines paramagnetischen Stoffes im Magnetfeld verlaufen mehr Feldlinien in die gleiche Richtung als ausserhalb – und der Paramagnet wird in das Magnetfeld hineingezogen, wenn auch nicht sehr stark.
Zudem gilt, ebenso wie für Diamagneten: Sobald das „fremde“ Magnetfeld verschwindet, gewinnt die Wärme, die ständig alle Atome bewegt, die Oberhand und schüttelt die Elementarmagnete in die Unordnung zurück.
Zu den paramagnetischen Stoffen zählen jene Elemente, deren Atome ungepaarte Elektronen, das heisst solche ohne Gegenstück in Sachen Orientierung, enthalten: zum Beispiel die Alkali- und Erdalkalimetalle und die seltenen Erden. Unter den Molekülen sind dementsprechend Radikale (die mindestens ein ungepaartes Elektron besitzen) paramagnetisch – so zum Beispiel Sauerstoff oder Stickstoffdioxid.
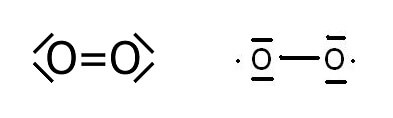
Bekannt ist die linke Darstellung des Sauerstoffmoleküls. Dass Sauerstoff paramagnetisch ist, lässt jedoch darauf schliessen, dass auch die rechte Darstellung mit zwei ungepaarten Elektronen der Wahrheit nahekommt.
Ferromagnetismus
Die Stoffe, die wir im Allgemeinen als „magnetisch“ kennen und aus welchen wir unsere Dauermagnete herstellen, verhalten sich im Prinzip wie Paramagnete. Allerdings ist der Ordnungs-„Sinn“ ihrer Elementarmagnete ungleich stärker, sodass Magnetfelder einen ungleich stärkeren Einfluss auf sie haben als auf Paramagnete.
Der bekannteste ferromagnetische Stoff ist Eisen (lateinisch Ferrum) – daher der Name für diese Art von Magnetismus. Ein Ferromagnet verstärkt nicht nur ein „fremdes“ Magnetfeld ungemein. Seine Elementarmagnete können ihre Ordnung zudem auch nach dem Verschwinden des ordnenden Magnetfeldes beibehalten, sodass „ihr“ Stoff dauerhaft ein Magnetfeld erzeugt!
Der verstärkte Ordnungssinn eines Ferromagneten rührt daher, dass die Elementarmagnete darin in besonders enger Beziehung zueinander stehen, welche ihnen eine besondere Austauschwechselwirkung ermöglicht. Diese Wechselwirkung beruht auf dem Pauli-Prinzip, das manch einer vielleicht aus der Schule kennt:
Zwei Elektronen mit vollkommen gleichen Eigenschaften dürfen nicht am gleichen Ort sein (deshalb haben zwei Elektronen, die sich ein Orbital im Atom teilen, stets entgegengesetzte Spins). Tatsächlich geht das Pauli-Prinzip aber noch weiter: Elektronen müssen sich stets in einer oder drei Eigenschaften unterscheiden, während zwei Unterschiede nicht erlaubt sind.
Werden also Elementarmagnete in enger Beziehung in einem Magnetfeld ausgerichtet, sodass ihre Orientierungen sich gleichen, unterscheiden sie sich nur noch in ihrem Ort. In Folge dessen ist ein zweiter Unterschied, zum Beispiel durch eine veränderte Orientierung, ohne das automatische Auftreten eines dritten Unterschiedes nicht mehr erlaubt. Ein Elementarmagnet im ausgerichteten Ferromagneten kann sich also nicht einfach so wieder umdrehen – auch dann nicht, wenn das ausrichtende fremde Magnetfeld längst wieder verschwunden ist.
Erst wenn die Wärmebewegung im Ferromagneten überhand nimmt, kann sie die Elementarmagnete aus ihrer „militärischen“ Starre reissen. Deshalb verlieren Dauermagnete bei hohen Temperaturen ihre Magnetkraft – die „Curie-Temperatur“ eines dauerhaft magnetischen Stoffs verrät, wann das der Fall ist (alternativ kann auch ein heftiger Schlag gegen den Magneten oder ein starkes, störendes Magnetfeld für entsprechende Unordnung sorgen).
Neben Eisen sind einzig die Elemente Cobalt und Nickel ferromagnetisch. Die Dauermagnete unseres Alltags bestehen zudem aus Legierungen, also Metallgemischen, die erst durch die Mischung ferromagnetisch werden.
Antiferromagnetismus
In manchen eigentlich ferromagnetischen Stoffen sind die Elementarmagnete in verschiedene Gruppen bzw. „Gitter“ eingeteilt, von welchen die eine Hälfte sich im Magnetfeld dank der Austauschwechselwirkung stabil in die eine Richtung ausrichtet, die andere Hälfte jedoch in die entgegengesetzte Richtung. Folglich erhält man, wenn man die Magnetkraft aller Elementarmagnete addiert, überhaupt keine Magnetkraft für einen solchen Stoff, und somit auch keine Wechselwirkung mit dem „fremden“ Magnetfeld. Zu diesen Antiferromagneten gehören unter anderem die Elemente Chrom und Mangan und das Mineral Hämatit.
Ferrimagnetismus
Verhalten sich die Elementarmagnete eines Stoffes im Grunde genommen wie die eines Antiferromagneten, während die Stärke ihrer Magnetfelder unterschiedlich ist, bleibt trotz entgegengesetzter Ausrichtung der verschiedenen Gitter ein Magnetfeld erhalten. Ein Ferrimagnet verhält sich also wie ein schwacher Ferromagnet – und tatsächlich gehören die ersten von Menschen entdeckten Dauermagnete in diese Gruppe:
Der Begriff „Magnet“ kommt nämlich vom griechischen „lithos magnes“, also „Stein aus Magnesia“, was sich auf die gleichnamige Region in Thessalien oder auch den Ort Magnesia am Mäander in der heutigen Türkei bezieht, welchen die „Magneten“ (nicht die Steine, sondern das Volk aus Thessalien!) gegründet haben sollen. Der ferrimagnetische Stein, welcher dort gefunden wurde, ist heute als das Mineral Magnetit, oder auch Magneteisenstein, bekannt. Es handelt sich dabei um das Eisenoxid Fe3O4 bzw. Fe(II)Fe(III)2O4, welches sowohl Fe2+– als auch Fe3+-Ionen enthält. Auch einige ähnliche Verbindungen, in welchen das Fe2+-Ion durch andere Metallionen ersetzt ist, sind ferrimagnetisch, und werden als Gruppe der „Ferrite“ zusammengefasst.

Magnetit (silbergraue Oktaeder) in Chalkopyrit (goldfarben) aus Aggeneys, Südafrika – ein ferrimagnetisches Mineral (by Rob Lavinsky, iRocks.com – CC-BY-SA-3.0 [CC BY-SA 3.0], via Wikimedia Commons)
Wie man einen Magneten herstellt
Wenn du einen Dauermagneten zur Hand hast, kannst du eine Eisennadel ganz einfach magnetisieren: Streiche dazu rund 50 mal mit dem Dauermagneten über die Eisennadel – immer in die gleiche Richtung! Auf diese Weise werden die Elementarmagnete in der Nadel nach und nach in die gleiche Orientierung „gebürstet“. Wenn du die Nadel schliesslich mit Hilfe eines Stücks Kork auf Wasser zum Schwimmen bringst, wird sie sich nach dem Erdmagnetfeld ausrichten.
Für die industrielle Herstellung von Magneten wäre es jedoch viel zu mühsam, jeden Magneten einzeln magnetisch zu bürsten. Deshalb verwenden die Hersteller von Dauermagneten ferro- oder ferrimagnetisches Pulver, welches sie innerhalb eines starken Magnetfeldes zusammenpressen. Für die schwarzgrauen, steinartigen Küchenmagnete werden dabei pulverisierte Ferrite eingesetzt. Da jedes Pulverkorn dabei einen Elementarmagnet darstellt (nicht so klein wie die „echten“ Elementarteilchen, aber klein genug), richten sich die Pulverkörner in diesem Magnetfeld ordentlich aus, ehe sie richtig zusammenpappen. Anschliessend werden die Pulverkörner bei sehr hohen Temperaturen zusammen geschmolzen (gesintert)…
Richtig! Dabei geht die Magnetkraft der einzelnen Körner und damit des ganzen Magneten aufgrund der heftigen Wärmebewegung der wirklichen Elementarmagnete wieder verloren! Allerdings bleibt die Orientierung der Körner selbst erhalten, sodass die Ordnung der Elementarmagnete nach dem Abkühlen in einem zweiten äusseren Magnetfeld problemlos wieder hergestellt werden kann.
Besonders starke Magnete erhält man zudem, wenn man dem ferromagnetischen Pulver einen paramagnetischen Stoff wie das Seltenerd-Metall Neodym unterjubelt: Die paramagnetischen Neodym-Teilchen werden im Magnetfeld des sie umgebenden Magnet-Pulvers dauerhaft in Ordnung gehalten und verstärken so das Magnetfeld des Dauermagneten ungemein!
Unglücklicherweise sind Seltenerd-Atome ziemlich reaktionsfreudig. Deshalb werden neodymhaltige „Supermagnete“ mit einer Schicht aus edleren Metallen (was diese Metalle edel macht ist eine andere Geschichte), in der Regel mit einer silbrig glänzenden Legierung aus Kupfer und Nickel, umgeben. Diese Beschichtung kann zudem vergoldet (dann glänzt der Magnet golden) oder verchromt werden.
Magnetismus und Strom
Die Maxwell-Gleichungen haben es bereits gezeigt: Wo ein Magnetfeld bewegt wird oder sich verändert, entsteht stets ein elektrisches Feld, und wo elektrische Ladungen (jede davon erzeugt ein kleines elektrisches Feld!) bewegt werden, entsteht ein Magnetfeld.
Diese Umstände weiss sich der Mensch zunutze zu machen, indem er einen Dauermagneten im Kreis dreht, sodass in seiner Umgebung Elektronen (in einem Draht) in Bewegung geraten (das ist ein Dynamo – oder im Grossformat ein Generator), oder Strom durch einen aufgewickelten Draht leitet, sodass das entstehende Magnetfeld in einem äusseren Magnetfeld mitsamt der Drahtspule in Drehung gerät (das ist dann ein Elektromotor). Die Einzelheiten zu solchen Elektromagneten und ihrem Nutzen bieten genug Stoff für eine eigene Geschichte und würden hier den Rahmen sprengen.
Im Allgemeinen unterscheidet sich das Magnetfeld eines Elektromagneten nicht von dem eines Dauermagneten – ausgenommen ist ein entscheidender Punkt: Sobald man einem Elektromagneten den Strom abstellt, verschwindet auch das Magnetfeld. Einen Dauermagneten kann man hingen nicht einfach ein- und ausschalten.
Das gilt auch für den grössten Magneten der Erde – die Erde selbst! Zwar ist das Erdmagnetfeld im weitesten Sinne auf einen riesigen Elektromagneten zurück zu führen – es wird von flüssigem Eisen erzeugt, welches im äusseren Erdkern in Strömungen bewegt wird – aber so lange unser Planet nicht innerlich auskühlt und erstarrt, wird nichts und niemand im Erdkern den Strom abstellen können. Und bis die Erde auskühlt, werden noch einige Milliarden Jahre vergehen müssen.
Elektromagnetische Wellen
Erst die untrennbare Verbindung zwischen elektrischen und Magnetfeldern ermöglicht uns, unsere Umgebung zu sehen und spannende Artikel über Magnetismus zu lesen. Denn wenn irgendwo in einem Atom ein Elektron zu schwingen anfängt, gerät eine elektrische Ladung in Bewegung – schliesslich schwingt die Elementarladung des Elektrons fleissig hin und her.
Und wo eine Ladung, und mit ihr ein elektrisches Feld in Bewegung ist, entsteht laut Maxwells Gleichungen ein Magnetfeld. Und wo ein Magnetfeld entsteht – was einer Veränderung desselben gleich kommt – entsteht sogleich wieder ein elektrisches Feld, und aus dem elektrischen Feld ein neues Magnetfeld…. Die Folge davon: die erscheinenden (und bei Ende der jeweiligen Veränderungen ebenso schnell wieder verschwindenden) Felder pflanzen sich durch den Raum fort. Und zwar so schnell wie nichts anderes: Die sich fortpflanzenden Felder bilden „elektromagnetische Wellen“ – kurz gesagt: Licht.
Und so, wie Licht durch bewegte elektrische Ladungen entsteht, können die Felder einer Lichtwelle wiederum Ladungen in Bewegung setzen. Wie uns dieser Umstand ermöglicht zu sehen, erfährst du in der Geschichte um Licht und Farben.
Supraleiter – die stärksten Magneten der Welt
Während Dauermagnete in ihrer Stärke durch die festgelegten magnetischen Eigenschaften ihrer Elementarmagnete begrenzt sind, hängt die Stärke eines Elektromagneten von der Stärke des darin fliessenden Stromes ab: Je stärker der Strom, desto stärker ist auch das erzeugte Magnetfeld. Theoretisch jedenfalls. Denn gewöhnliche Drähte leisten dem Strom stets einen gewissen Widerstand – dadurch entsteht im Draht „Reibungswärme“, die mit zunehmender Stromstärke irgendwann jedes Material zerstört.
Fast jedes Material zumindest. Denn glücklicherweise (für Physikfans und die moderne Technik) haben Wissenschaftler in den 1980er Jahren entdeckt, dass manche Materialien bei sehr, sehr niedrigen Temperaturen kurzerhand ihren gesamten Widerstand aufgeben – und somit ohne Reibung elektrischen Strom leiten. Die ersten dieser Supraleiter mussten noch mit flüssigem Helium auf unter 4°C über dem absoluten Nullpunkt gekühlt werden. Inzwischen gibt es jedoch sogenannte „Hochtemperatur“-Supraleiter, die sich schon mit flüssigem Stickstoff (bis -196°C, also rund 77°C über dem absoluten Nullpunkt) zufrieden geben. Und der lässt sich vergleichsweise wirtschaftlich beschaffen.
Deshalb werden die stärksten Elektromagneten, die beispielsweise in Kernspintomographen oder in Teilchenbeschleunigern zum Einsatz kommen – oder in Labors fantasievoller Wissenschaftler, die Frösche zum Schweben bringen, aus supraleitenden und damit nicht durchbrennenden Drähten hergestellt.
Noch spektakulärer anzuschauen sind wohl die Folgen einer weiteren Eigenschaft der Supraleiter: Neben der unbegrenzten Leitfähigkeit sind sie nämlich auch vollkommene Diamagneten – was ihnen ermöglicht, in einem ausreichend starken Magnetfeld frei zu schweben:
(Nicht zur Nachahmung empfohlen: Flüssigen Stickstoff oder damit Gekühltes NIEMALS mit der blossen Hand anfassen – Kaltverbrennungsgefahr!)
Sind Magnete oder Magnetfelder gefährlich?
Nach unserem heutigen Wissensstand: Nein. Die Orientierung der Elementarmagnete im menschlichen Körper ist für die Funktion der Atome und Moleküle darin praktisch ohne Bedeutung. Menschen bekommen daher selbst dann kaum etwas davon mit, wenn sie in ein starkes Magnetfeld geraten – wie ich nach einer Kernspin-Tomographie meines Kopfes vor einigen Jahren bestätigen kann. Einzig ein paar Lichtblitze „vor“ meinen Augen – so genannte „Magnetophosphene“, die durch Beeinflussung der Nervenströme in der Netzhaut durch das Magnetfeld entstehen – haben auf die Existenz des Feldes hingewiesen.
Anderes gilt für elektrische Geräte jeder Art: Da elektrische Ströme mit Magnetfeldern wechselwirken, können letztere elektrische Geräte gehörig durcheinander bringen oder sogar ausser Gefecht setzen. Wer einen Herzschrittmacher trägt, sollte sich also tunlichst von Kernspintomographen oder Supraleiter-Labors fernhalten (und nicht nur davon – selbst im Schullabor, wo einfache Magnet-Rührgeräte zum Einsatz kommen, habe ich das Warnschild für Herzschrittmacher-Träger gesichtet).
Darüber hinaus besteht die grösste Gefahr, die von Magneten ausgeht, wohl darin, sich unter starken Neodym-Magneten Körperteile einzuquetschen oder von plötzlich im Magnetfeld herumfliegenden ferromagnetischen Gegenständen getroffen zu werden.
Du kannst dich also getrost von der geheimnisvollen Magnetkraft verzaubern lassen und nach Herzenslust mit Magneten experimentieren.
Oder hast du schon? Welche Erfahrungen hast du mit Magneten schon gemacht?