Dieser Artikel enthält Affiliate-Links aus dem Affilinet-Partnerprogramm des Orell-Füssli-Verlags (gekennzeichnet mit (*) – (*) ) – euch kosten sie nichts, mir bringen sie vielleicht etwas für meine Arbeit ein. Ich habe für diese Rezension vom Orell Füssli Verlag ein Rezensionsexemplar des Buches und eine Zusage für den Versand eines zweiten Exemplars als Gewinn erhalten. Vielen Dank dafür! Es besteht kein Interessenkonflikt hinsichtlich des Inhalts in diesem Beitrag und dessen Publikation.
Mint&Malve veranstalten anlässlich des ersten Schweizer Vorlesetages am 23.Mai – ausgerichtet vom Schweizerischen Kinder- und Jugendmedien SIKJM – die Blogparade #vorlesefieber , bei welcher sich alles ums Vorlesen dreht. Vorlesen – das ist eine wunderbare Möglichkeit, Zeit mit (seinen) Kindern zu verbringen und sie von Anfang an beim Lernen zu unterstützen – ohne dass die Kinder etwas davon merken! Denn Vorlesen fördert Sprachkompetenz und Kreativität… und kann nebst Nähe auch noch Wissen vermitteln. Um zum Vorlesen und Zuhören zu animieren, finden an 23. Mai in der ganzen Schweiz Veranstaltungen rund ums Vorlesen statt – und hier in der virtuellen Schweiz bloggen wir fleissig zu allem, was eine schöne Vorleserunde ausmacht.
Aber wie passen denn Vorlesen und Naturwissenschaft zusammen? Kann man denn Kindern überhaupt schon so etwas wie Chemie vermitteln? Und sind Lehrbücher nicht selbst dann, wenn sie vorgelesen werden, viel zu trocken für junge Forscher?
Mitnichten! Ich war selbst positiv überrascht als ich zum ersten Mal davon las: Es gibt tatsächlich Kinderbücher, welche den jungen und jüngsten Lesern die Chemie ihrer Alltagswelt näher bringen und zum Erforschen anregen – und das ganz ohne den üblichen negativen Anstrich meines Fachs! Eines davon ist noch dazu made in Switzerland und dreht sich um einen der grössten Helden der Schweizer Kinderliteratur: Ich schreibe von „Chemie mit Globi“!
Globi forscht und entdeckt
…und seine Fans forschen und entdecken mit. In diesem Band der Reihe GlobiWissen macht der stets neugierige Globi sich daran, die Chemie in seiner alltäglichen Umgebung (schliessich ist Chemie überall und alles ist Chemie) zu erforschen. Dabei unterstützt ihn sein Freund, der Chemieprofessor Justus K. Rauch, nach Kräften. Und hinter Justus verbergen sich eine ganze Reihe kluger Chemieprofessoren und Gymnasiallehrer, die im Auftrag der Akademie der Naturwissenschaften Schweiz gründlich darauf geschaut haben, dass alles seine chemische Richtigkeit hat und verständlich ist.
So sind fast 100 farbenfrohe Seiten entstanden, auf welchen Globi und Justus ihre Welt der Stoffe und Reaktionen erkunden – die der Alltagswelt jeder Familie entspricht. Und das Beste ist: Sie verraten sogar, wie man einige ihrer Experimente nachmachen kann, sodass die Leser (bzw. Zuhörer) auch selbst mitexperimentieren können!
Zum Inhalt des Buches
Die Chemie ist ein unglaublich weites Feld, und tatsächlich geht in unserem Leben und unserer Umgebung praktisch nichts ohne sie (denn auch das Leben selbst und die Natur beruhen letztlich auf Chemie). Dementsprechend vielfältig und weit gestreut sind auch die Inhalte von „Chemie mit Globi“. Deshalb gebe ich euch eine Kurzübersicht, was ihr in diesem Buch finden könnt. Und zu fast allen Themen gibt es überdies Experimentieranleitungen zum Selberforschen!
- Einleitung – ganz nach dem Motto von Keinsteins Kiste: Chemie ist überall – alles ist Chemie – und ein Wimmelbild-Inhaltsverzeichnis
- Geschichte der Chemie, und ein wichtiger Sicherheitshinweis für alle folgenden Experimente
- Atome und Elementarteilchen, Periodensystem der Elemente
- Verbindungen: das Wassermolekül und Reaktionsgleichungen
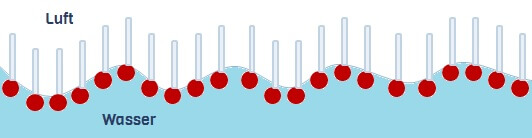
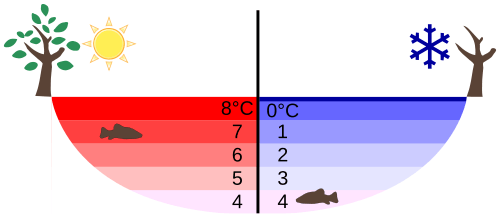
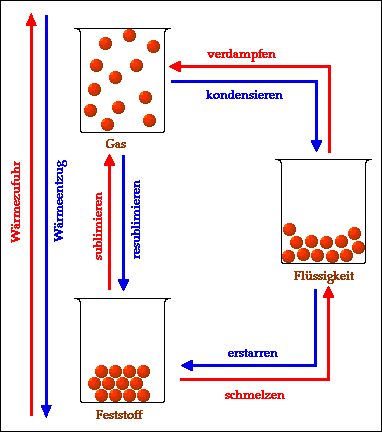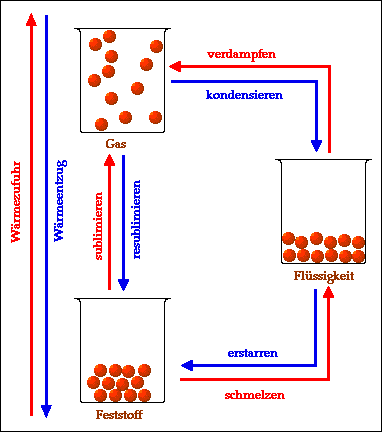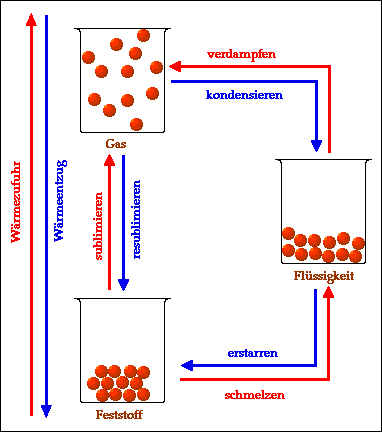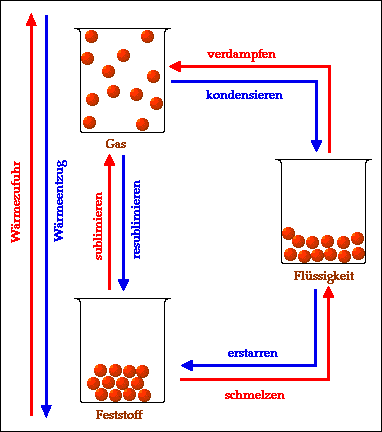
- Die Aggregatzustände fest, flüssig und gasförmig und ihre Umwandlungen ineinander
- Reinstoffe, Stoffgemische und Trennverfahren
- Metalle, Legierungen, Edelmetalle
- Säuren und Basen (unter anderem mit dem Versuch mit dem „nackten Ei“) und die Messung des pH-Werts (als Experiment mit Rotkohl)
- Salze und ihre Flammenfarben, die zum Beispiel dem Feuerwerk seine Farben geben
- Die Entstehung von Rost
- Die verschiedenen Erscheinungsformen von Kohlenstoff, Kohlenstoff als Element des Lebens, fossile Brennstoffe
- Düngemittel und Nährstoffkreislauf in der Natur
- Kunststoffe aus Erdöl: Langlebigkeit, Recycling
- Strom durch Chemie: Batterien, Recycling, Leitfähigkeit von Salzlösungen
- Medikamente sind Chemikalien
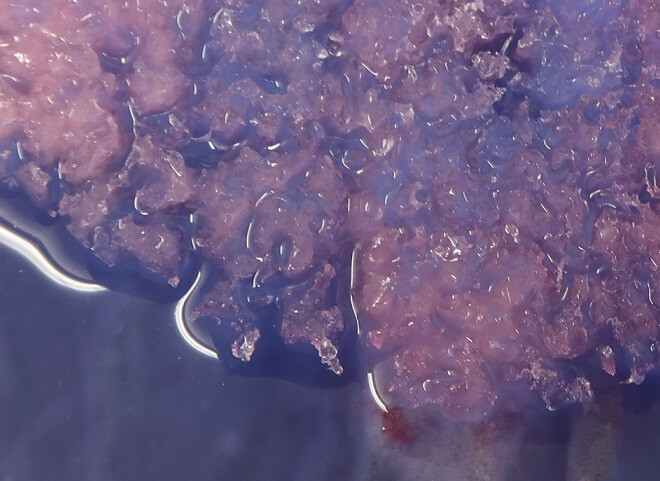
- Gele: Gelatine als Superabsorber, Leim und Klebstoffe
- Hefen machen Chemie: Sie erzeugen neue Stoffe, z.B. das Gas Kohlendioxid, Gärung
- Indigo und andere pflanzliche Farbstoffe
- Seife und die Superwaschkraft
- Duft- und Aromastoffe aus der Natur
- Spurensuche dank Erbsubstanz: DNA in der Kriminaltechnik
Zu guter Letzt werden reale ChemikerInnen vorgestellt – wie sie an Universitäten und vielen anderen Betrieben arbeiten, und solche, die weltberühmt geworden sind. So ist es fast unumgänglich, dass die Lektüre Neugier geweckt hat. Und Globi wäre vermutlich nicht Globi, wenn er nicht noch Infos zur Hand hätte, wo ihr euch weitergehend über Chemie-Berufe informieren oder weiter über Chemie und Experimente nachlesen könntet.
Und dass ihr aufmerksam gelesen bzw. beim Vorlesen zugehört habt, könnt ihr auf der letzten Seite des Buches schliesslich mit Globis Chemie-Quiz beweisen.
Mein Eindruck vom Buch
Auf knapp 100 Seiten wird eine grosse Fülle von Themen und Alltags-Phänomenen, die einen vielfältigen Einblick in das unfassbar weite Feld der Chemie gewähren, vorgestellt. Dabei schauen die Autoren nicht davor, auch abstraktere Inhalte wie Elementarteilchen, Elementsymbole und Reaktionsgleichungen einzubringen.
Warum auch – schliesslich haben auch und gerade solche alltagsfremden Dinge grosses Potential, um Neugier zu wecken. So haben mich selbst schon ab 8 Jahren in meinem WasistWas-Buch über Sterne und Astronimie die Skizzen zur Kernfusion mit dem Teilchenmodell am meisten fasziniert. – Indem diese Neugier genutzt wird, wird den Kindern ein einfacher Zugang zu später oft als „schwierig“ weil „abstrakt“ verschrienen Inhalten ermöglicht. Nichts desto trotz bleibt die Chemie mit Globi stets leicht verständlich.
So können auch die Grossen, die kaum (noch) Ahnung von Chemie haben, beim gemeinsamen (Vor-)Lesen und Experimentieren entdecken und repetieren – und sich so für allfällige Fragen widmen. Die werden nämlich ganz sicher kommen. Denn Globi und die Chemie ist kein umfassendes Lehrbuch – es macht vielmehr neugierig und regt dazu an, sich ohne negativen Vorbehalt mit der spannenden Chemie des Alltags zu beschäftigen.
Eckdaten zum Buch
(*)
Chemie mit Globi – Globi forscht und entdeckt
(*)
Globi-Verlag, Imprint Orell Füssli Verlag AG, Schweiz 2011
Hardcover-Ausgabe, 96 Seiten
ISBN 978-3-85703-007-9
Fazit
Chemie vorlesen? Ja, das geht! Das Buch richtet sich zwar vornehmlich an Kinder der Primarstufe (1. bis 6. Klasse), die also schon selbst lesen können oder lernen, aber auch in diesem Alter verbindet das gemeinsame Lesen. Denn manchmal ist es einfach entspannter, jemandem zuzuhören – und diesen Jemand dann auch gleich mit Fragen eindecken zu können, als selbst zu lesen. Und ich habe schon Kindergärtler kennengelernt, die ihre Eltern mit Fragen zu „Ha-zwei-Oh“ gelöchert haben (und die Eltern waren dann froh, bei mir und in Keinsteins Kiste Antworten auf so manche Frage zu finden).
Im Übrigen: Niemand ist perfekt…auch nicht Globi. So haben sich aller Umsicht und Mühe zum Trotz ein paar Fehler in diesen Band eingeschlichten. Macht aber nichts, denn der Orell Füssli Verlag bietet die korrigierten Seiten gratis zum Download an. Und wenn ihr euch schon ein wenig mit Chemie auskennt: Findet ihr den groben Fehler gleich auf dem Cover (dem Beitragsbild)? Die Auflösung und alle anderen korrigierten Seiten findet ihr hier!
Gewinnspiel: Chemie mit Globi für euch
Wenn ihr nun neugierig seid und die Chemie mit Globi erforschen möchtet, habe ich noch ein besonderes Schmankerl für euch: Der Orell Füssli Verlag stellt mir ein Exemplar von „Chemie mit Globi“, das ich unter euch verlosen darf! Herzlichen Dank dafür!
Wie ihr am Gewinnspiel teilnehmen könnt
Zur Teilnahme kommentiert diesen Beitrag mit gültiger E-Mail-Adresse (die brauche ich, um euch über euren Gewinn benachrichtigen zu können!) und schreibt, welche Alltagsbeobachtung euch besonders neugierig auf Chemie, Physik und Co macht, oder was euch mit Globi verbindet.
Teilnahmebedingungen
- Das Gewinnspiel wird von Keinsteins Kiste in Zusammenarbeit mit dem Orell Füssli Verlag veranstaltet. Vielen Dank für die Bereitstellung und den Versand des Preises!
- Das Gewinnspiel startet am 15. Mai 2018 und endet am 31. Mai 2018 um 24.00 Uhr.
- Die Teilnahme am Gewinnspiel ist kostenlos.
- Ihr müsst mindestens 18 Jahre alt sein (Liebe Kinder: Tut euch mit euren Eltern, Grosseltern oder anderen Erwachsenen zusammen!).
- Ihr müsst eine Post-Adresse in der Schweiz, Deutschland oder Österreich haben, an welche der Gewinnpreis versandt werden kann.
- Gewinnpreis ist ein Exemplar des Buches „Chemie mit Globi“.
- Es gibt 1 Los für einen Kommentar mit gewünschtem Inhalt (s.o.).
- Eine Auszahlung des Gewinns in bar ist nicht möglich. Der Rechtsweg ist ausgeschlossen.
- Der Gewinner wird ausgelost und per eMail benachrichtigt. Dabei wird er darum gebeten, der Weitergabe seiner Postadresse an den Orell Füssli Verlag zuzustimmen, damit der Gewinn direkt vom Verlag versandt werden kann.
- Die Gewinne gelten auf den Namen der teilnehmenden Person und sind nicht auf Drittpersonen übertragbar. Sofern die Ausschüttung eines Gewinns an einen in der Ziehung ermittelten Gewinner nicht möglich ist, weil eine Gewinnbenachrichtigung und/oder Gewinnzustellung scheitern und nicht binnen eines Monats nach der Ziehung nachgeholt werden können, verfällt der Gewinnanspruch.
- Der Veranstalter behält sich das Recht vor, das Gewinnspiel aus sachlichen Gründen jederzeit ohne Vorankündigung zu modifizieren, abzubrechen oder zu beenden.
Und nun wünsche ich euch viel Spass beim (Vor-)Lesen, Forschen, Experimentieren und Mitspielen!