Gestern wurden die Nobelpreise für 2019 vergeben: Der Nobelpreis für Chemie geht an John B. Goodenough, M. Stanley Whittingham und Akira Yoshino – für eine wahrhaft weltbewegende Erfindung: Den Lithium-Ionen-Akku.
Ein Preis für den grössten Nutzen für die Menschheit
Der schwedische Erfinder und Industrielle (u.A. Erfinder des Dynamits) Alfred Nobel verfügte vor seinem Tod am 10. Dezember 1896 in seinem Testament, dass von seinem riesigen Vermögen eine Stiftung gegründet werde, deren Zinsen „als Preis denen zugeteilt werde, die im verflossenen Jahr der Menschheit den grössten Nutzen geleistet haben“. Das Preisgeld wird zu gleichen Teilen in den Bereichen Physik, Chemie, Medizin bzw. Physiologie, Literatur und Friedensbemühungen vergeben*.
*Der ebenfalls oft genannte „Wirtschaftsnobelpreis“ ist dagegen kein „echter“ Nobelpreis: Er heisst eigentlich Alfred-Nobel-Gedächtnispreis für Wirtschaftswissenschaften und wird erst seit 1968 von der Schwedischen Reichsbank gestiftet.
Die Nobelpreise werden seit 1901 bis heute vergeben (teils mit Verspätung oder Auslassung, wenn kein würdiger Träger gefunden wurde oder ein Weltkrieg dazwischen kam). Dabei wird in jüngerer Zeit längst nicht mehr Leistungen des jüngsten „verflossenen“ Jahres ausgezeichnet. Stattdessen wird Erfindungen und Bemühungen – besonders in den wissenschaftlichen Disziplinen – Zeit gegeben, ihre Bedeutung für die Menschheit zu beweisen.
Wie Lithiumionen-Akkus die Welt verändert haben
So werden auch die Träger des Nobelpreises für Chemie 2019 für Leistungen geehrt, die sie in den 1970er und 1980er Jahren vollbracht haben. Und die haben wahrhaftig unsere Welt verändert!
Eine Zeit ohne Hochleistungs-Akkus
Wenn ihr mindestens so alt seid wie ich (ich bin Anfang der 1980er Jahre geboren), werdet ihr euch noch an die Zeit erinnern, als Einwegbatterien meist giftiges Cadmium enthielten, wenig Leistung lieferten und eine geringe Lebensdauer hatten. Tragbare Kassettenspieler hatten monströse Batterieschächte, lichtstarke Taschenlampen konnten als Totschläger zweckentfremdet werden und leistungsstärkere Elektrogeräte gab es nur fest verortet an der Steckdose.
Wiederaufladbare Batterien, sogenannte Akkus, waren der neueste Schrei. Die ersten Vertreter ihrer Art waren schwere Brocken, denn sie enthielten ebenso giftiges wie schweres Blei. Die Nickel-Metallhydrid-Akkus, an die ich mich aus meinen letzten Jugendjahren noch erinnere, enthielten ebenfalls ein giftiges Schwermetall – Nickel – und konnten, bei nur wenig geringerem Gewicht, in ihrer Kapazität auch nicht mit den Einweg-Batterien mithalten.
1991 kam der Lithium-Ionen-Akku auf den Markt – und erst Jahre später in meine Welt. Nämlich Mitte der 1990er verbaut in Papas erstem tragbaren PC – pardon, „Laptop“, von seinem damaligen Arbeitgeber. Der wog dereinst noch rund 4 Kilogramm – konnte aber, was jeder Office-PC an der Steckdose leistete! Darauf folgte sein erstes Mobiltelefon…und schon kurz darauf, um das Jahr 2000, konnte ich mir schon ein handliches Pre-Paid-Handy vom Schülerinnen-Taschengeld leisten.
Die neue Welt der Mobilität
Heute schreibe ich diesen Artikel an meinem modernen Convertible, der gerade einmal ein Kilo wiegt und trage einen Taschencomputer mit Telefonfunktion, der kleiner als eine Tafel Schokolade ist und mehr Rechenleistung aufbringt als Papas 4-kg-Laptop von damals, im Dauerbetrieb mit mir herum. Und das einen ganzen Tag lang.
Mein Lieblings-Autovermieter hat mir unlängst als nette Zusatzüberraschung ein Hybrid-Fahrzeug ausgehändigt, dessen Akku über den Dynamo im Verbrennungsmotor aufgeladen wird und damit langsame Fahrt mit einem Elektromotor machen kann. Auch im vollständig elektrisch betriebenen Tesla bin ich schon ein kleines Stück mitgefahren.

(by ENERGY.GOV [Public domain], via Wikimedia Commons)
Die Garage des Tesla-Besitzers mag statt mit Schindeln mit Solarzellen, die aus Sonnenenergie Strom erzeugen und in einen grossen „Tankstellen-„Akku speisen, gedeckt sein.
Besonders diese letzten Entwicklungen mögen die Jury zur Vergabe des Preises bewegt haben:
„Sie haben die Grundlage gelegt für eine drahtlose, von fossilen Brennstoffen freie Gesellschaft und sind für die Menschheit von größtem Nutzen.“
Aber wie funktioniert eigentlich ein Lithium-Ionen-Akku?
Im Grunde genommen ist ein Akku (-mulator) eine Spielart der Batterie, nämlich eine wiederaufladbare Batterie.
Was ist eine Batterie?
Eine Batterie im Allgemeinen ist ein Speicher für elektrischen Strom. Da „elektrischer Strom“ ein Strom aus negativ geladenen Teilen, den Elektronen, ist, bedeutet das: Eine Batterie ist ein Behälter, in welchem Elektronen getrennt von positiven Ladungen aufbewahrt werden.
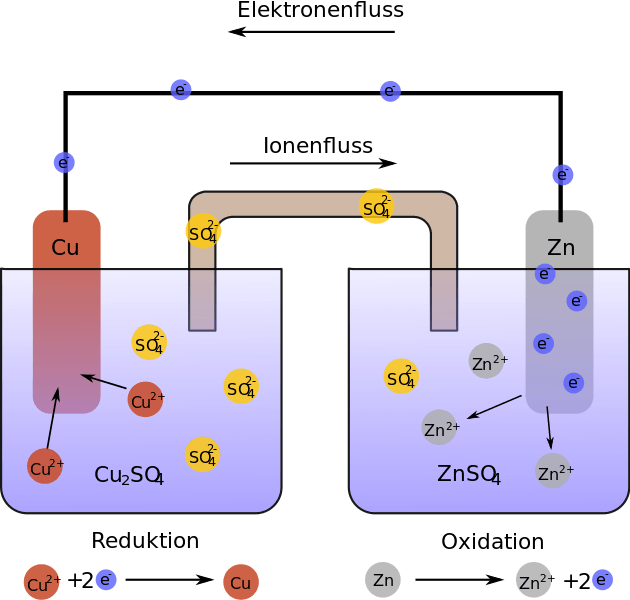
(by Myukew [CC BY-SA 3.0], via Wikimedia Commons)
Nun lassen sich Elektronen nicht freiwillig von positiven Ladungen trennen (positive und negative Ladungen finden einander nämlich äusserst anziehend). Eine Batterie zu erschaffen erfordert dementsprechend Energie – die bei ihrer Benutzung in Form des elektrischen Stroms an das betriebene Elektrogerät weitergegeben wird.
Verbindet man die beiden Teilbehälter (die „Pole“ einer Batterie sind quasi Öffnungen dieser Behälter) miteinander, strömen die Elektronen, angezogen von den positiven Ladungen auf der anderen Seite, dem gegenüberliegenden Pol entgegen. Und zwar so lange, bis an beiden Polen die gleiche Ladung versammelt ist. Dann gibt es nichts mehr, was fliessen wollte, und die Batterie ist leer.
Wie man eine Batterie wieder auflädt
Einweg-Batterien sind so geschaffen, dass ihr Material endgültig „verbraucht“ ist, wenn die Ladungen an den beiden Polen erst einmal ausgeglichen sind. Sie müssen dann im Sondermüll entsorgt und aufwändig wiederverwertet werden. Deshalb waren wieder aufladbare Batterien von vorneherein erstrebenswert.
Solche müssen folglich aus Materialien bestehen, in welche man am negativen Pol neue Elektronen – aus einer Steckdose oder „frisch“ aus einem Generator – hinein stopfen kann, während man am positiven Pol Elektronen herauszieht. In den ersten Akkus enthielten solche Materialien Blei, in späteren Nickel – beides giftige Schwermetalle, deren Name zudem Programm ist (besonders Blei ist ja als Schwergewicht wohlbekannt).
Zudem war das Hineinstopfen von Elektronen in ein Material nicht eben einfach. Schliesslich stossen sich gleiche Ladungen ja gegenseitig ab, sodass viel Aufwand nötig ist, um viele davon eng gepackt in den gleichen Behälter zu pferchen.
Michael Stanley Whittinghams Idee
In den 1970er Jahren kam der Chemiker M. Stanley Whittingham auf die Idee, das Zusammenpferchen von Elektronen zu erleichtern, indem er positiv geladene Ionen in das eigentliche Material am Minuspol einwandern liess, die diese Elektronen entgegennehmen sollten.
Dazu bot sich Lithium, das leichteste aller Alkalimetalle (der Elemente ganz links im Periodensystem unterhalb vom Wasserstoff) geradezu an. Wie alle Alkalimetalle ist es nämlich nur zu gern bereit, die entgegengenommenen Elektronen wieder abzugeben, sobald sie gebraucht werden. Zudem sind seine Salze wasserlöslich und es besteht aus den leichtesten Metall-Atomen des Universums, sodass es leichte Batterien verspricht.
Redox-Chemie im Lithium-Ionen-Akku
Whittingham verwendete also Titandisulfid, TiS2, (auch das Metall Titan(ium) ist relativ leicht und vor allem ungiftig) als Elektrode am Pluspol, in welches Lithium-Ionen eingelagert waren. Beim Aufladen bewegte der Überschuss an positiver Ladung die Lithiumionen aus dem Material hinaus, sodass sie zum Minuspol, einem Stück Lithium-Metall, wandern konnten. Dort angekommen konnten sie ein in das Lithium gestopftes Elektron aufnehmen und sich als Metall-Atome zum übrigen Metall gesellen:
Vielleicht erinnert ihr euch noch daran: Eine Reaktion, bei der Elektronen aufgenommen werden, heisst Reduktion.
Zum Ausgleich werden am Pluspol Elektronen entfernt, sodass dort mehr positive Ladung verbleibt. Eine Reaktion wie diese, bei welcher Elektronen abgegeben werden, heisst übrigens Oxidation.
Wurde eine solche Lithiumbatterie über eine Ladevorrichtung mit einer Stromquelle verbunden, wurden also Elektronen aus Titandisulfid entnommen, während Lithium-Ionen von dort zur Lithium-Elektrode wanderten, um dort hineingestopfte Elektronen entgegen zu nehmen.
Nahm man dann die Stromquelle weg und verband die Pole stattdessen aussen herum mit einem Verbraucher (also ein Elektrogerät), gaben Lithium-Atome im Lithium-Metall ihre Elektronen wieder ab:
Die Lithium-Ionen wanderten zurück zum Titandisulfid, während die Elektronen durch den Verbraucher zurück zum Pluspol flossen und dabei das Gerät antrieben wie Wasser eine Mühle.
Wiederaufladbarkeit durch umkehrbare Reaktionen
Die Richtung der oben genannten Redox-Reaktionen wird nach dem Aufladen des Akkus bei seinem Gebrauch also einfach umgekehrt. Und sobald die Ladungen an den Polen ausgeglichen sind und der Akku damit „leer“ ist, wird die Reaktionsrichtung beim nächsten Aufladen erneut umgekehrt, und dann wieder und wieder.
Dieses Umkehren funktioniert viele Male, bevor es zu einem merklichen Verschleiss des Materials kommt. Nur: In Titandisulfid liessen sich zwar so einige Lithium-Ionen unterbringen, aber noch nicht genug, als dass die Batterien wirklich handlich gewesen wären.
Vom Plus- zum Minuspol gelangen die Lithiumionen übrigens durch einen Elektrolyten, also einen Stoff (flüssig oder fest), der Ionen (und damit eine Spielart des elektrischen Stroms) leiten kann. Der Elektrolyt verbindet Minus- und Pluspol miteinander, wobei eine nur teilweise passierbare Trennschicht („Separator“) dafür sorgt, dass das einen Kurzschluss gibt.
John Bannister Goodenough legt nach
Dem Physiker John B. Goodenough waren die Whittingham’schen Batterien deshalb nicht ‚gut genug‘. So forschte er weiter und entdeckte 1980, dass sich Lithiumcobaltoxid, LiCoO2, noch besser für den Pluspol eines Lithium-Ionen-Akkus eignet als Whittinghams Titandisulfid. Denn in das Ionengitter dieser Verbindung passen besonders viele Lithiumionen. Und diese können hinaus und hinein wandern, ohne dass das Gitter daran Schaden nimmt.
Damit liess sich eine doppelt so hohe Spannung in der neuen Batterie erzeugen wie mit der ursprünglichen Version von Whittingham!
Wenn Hitze zum Problem wird
Einen Haken hat das Material aber doch: Ab einer Temperatur von 180°C wird aus Lithiumcobaltoxid Sauerstoff freigesetzt. Und der ist als rücksichtsloser Elektronendieb (auf chemisch: starkes Oxidationsmittel) berüchtigt. So reagiert der freigesetzte Sauerstoff wild mit den Materialien des Akkus, der daraufhin lichterloh und unlöschbar abbrennt (Fachleute sagen: der Akku „geht thermisch durch“).
Das lässt sich aber relativ leicht verhindern, indem man dafür sorgt, dass der Lithium-Ionen-Akku nicht zu heiss wird.
Ein wesentlich grösseres Problem stellt dahingehend Lithium-Metall dar. Die Fähigkeit von Alkalimetallen wie Lithium, sehr leicht ein Elektron abzugeben (also oxidiert zu werden), die für die Lithiumbatterien so nützlich ist, führt nämlich auch dazu, dass diese Metalle sehr lebhaft mit allem Möglichen reagieren. Zum Beispiel mit Wasser.
So konnte schon ein wenig Feuchtigkeit dazu führen, dass die Whittingham’sche wie auch die Goodenough’sche Lithiumbatterie kaputt oder gar in Flammen aufging. Das war für eine Anwendung ausserhalb des Labors mit seinen Sicherheitsvorkehrungen natürlich nicht vertretbar.
Akira Yoshino liefert den (vorerst) letzten Schliff
Der Ingenieur Akria Yoshino fand 1985 schliesslich einen stabileren Ersatz für das impulsive Lithium-Metall am Minuspol: Er verwendete Petrolkoks, einen kohlenstoffreichen Abfall aus der Erdölverarbeitung, in welchen wiederum Lithiumionen (bzw. -atome) eingebettet werden. Eine Elektrode aus einem solchen Material tut ebenso ihren Dienst wie metallisches Lithium, geht aber nicht bei jeder Kleinigkeit in die Luft. Heutzutage wird stattdessen Graphit, also reiner Kohlenstoff, verwendet, der, anders als Petrolkoks, keine weiteren und giftigen Abfälle mehr enthält.
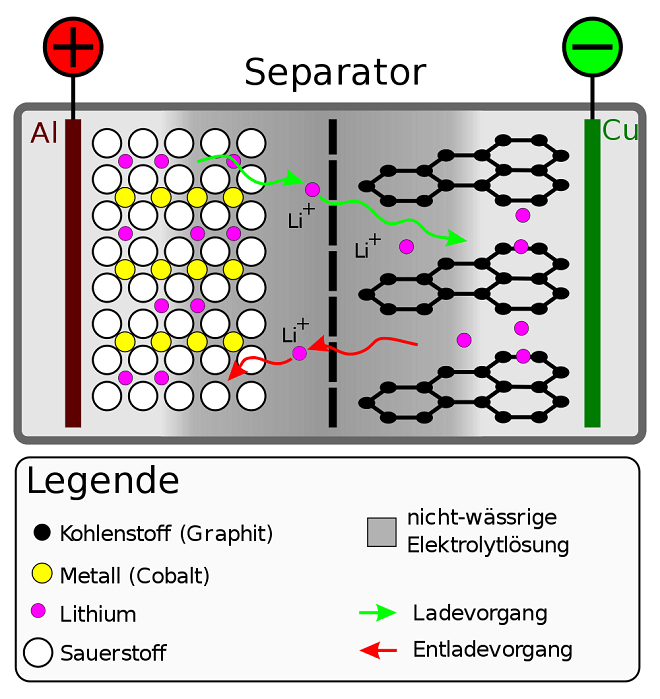
(by Cepheiden [CC BY-SA 2.0 de], via Wikimedia Commons )
Damit waren alle Zutaten zusammen, um einen für die Anwendung durch Otto Normalverbraucher sicheren Akku auf den Markt zu bringen. Der erste seiner Art kam dann auch 1991 in einer Videokamera der Firma Sony aus Yoshinos Heimatland Japan auf den Markt.
Sind Lithium-Ionen-Akkus wirklich sicher?
Immer wieder hört und liest man in den Medien von Lithium-Ionen-Akkus, die in Flammen aufgehen und Verletzungen oder grössere Brände verursachen. Dennoch sind solche Vorkommnisse Einzelfälle, die meist durch Beschädidungen der Batterien (durch die Sauerstoff in die Akkus gelangen kann) oder Baufehler (wie 2017 bei dem berüchtigten Samsung Galaxy Note 7) verursacht werden.
So könnt ihr verhindern, dass eure Lithium-Ionen-Akkus „durchgehen“
- Verwendet nur das Ladegerät, das für euren Akku bzw. euer Elektrogerät vorgesehen ist! So verhindert ihr, dass zu viele Elektronen hineingestopft werden und der Akku deshalb überhitzt.
- Zerlegt oder/und kombiniert Lithium-Ionen-Akkus niemals selbst! Eine intakte Umhüllung sorgt dafür, dass reaktionsfreudige Bestandteile des Akkus drinnen und Sauerstoff und Wasser draussen bleiben.
- Haltet eure Akkus und Geräte sowohl von Feuer und Hitze über 60°C (Sonneneinstrahlung!) als auch von Frost fern. Beide Extreme können zu Beschädigungen führen!
- Wenn ein Lithium-Ionen-Akku beschädigt oder verformt aussieht, benutzt ihn keinesfalls, sondern entsorgt ihn umgehend (als Sondermüll bzw. beim Hersteller oder Verkäufer des Geräts)! Ist der beschädigte Akku neu und habt ihr noch eine Garantie für das Gerät, bekommt ihr allenfalls kostenlos Ersatz dafür.
Und wenn euer Akku doch einmal kaputt ist oder gar brennt
- Die Lithium-Ionen-Akkus unserer Elektrogeräte enthalten kein metallisches Lithium. Wasser facht einen Brand eines solchen also nicht an, sodass ihr ein Gerät mit brennendem Akku und seine Umgebung getrost mit Wasser kühlen könnt. CO2– oder Schaum-Feuerlöscher könnt ihr ebenfalls verwenden.
- Löschen lässt sich ein durchgehender Lithium-Ionen-Akku aber nicht. Lasst ihn daher, wenn möglich, an einem feuerfesten Ort (und fern von eurem Körper) einfach ausbrennen.
- Droht ein Brand ausser Kontrolle zu geraten, ruft umgehend die Feuerwehr zur Hilfe (118 in der Schweiz, 112 in Deutschland und Österreich)!
- Sollte Flüssigkeit aus einem beschädigten Akku auslaufen, lasst sie nicht an eure Haut gelangen: Die Elektrolytflüssigkeit aus solchen Akkus kann mit Wasser zu äusserst giftiger Flusssäure reagieren! Fasst auslaufende Akkus nur mit Schutzhandschuhen und kürzestmöglich (die Handschuhe danach sofort ausziehen und entsorgen!) an, umwickelt sie mit mehreren Lagen Plastik oder bringt sie am besten noch im zugehörigen Gerät umgehend zur Sondermüllentsorgung!
Die Zukunft der wiederaufladbaren Batterien
Mit den bestehenden Schwachstellen sind die heutigen Lithium-Ionen-Akkus besonders einem ihrer Mit-Erfinder noch immer nicht ‚gut genug‘: Mittlerweile 97 Jahre alt (und damit der älteste Empfänger eines Nobelpreises aller Zeiten!) und kein Bisschen müde forscht John B. Goodenough bis heute an Neuerungen für wiederaufladbare Batterien.
Dabei zielen seine Neuentwicklungen darauf ab, das im Universum und damit auch auf der Erde relativ seltene Lithium durch seinen sehr viel häufigeren Bruder Natrium (dessen Ionen z.B. Bestandteil von Kochsalz sind) zu ersetzen.










